��
����ЧӦ����Դ���ս� Origin and Termination of Warburg Effct
��
�ֱ�ЧӦ����Դ
��Ŀ�ܽ
���ϸ����������������ATP���������ƣ�������������ǽͽⷢ�͡�ͨ��·��˹����˹�£�Louis Pasteur���Ŀ������о���������Ϊֻ��������������֧�ֺ���������£�����Ч�ʲŻή�͡�ֱ����Լ100��ǰ����Ȼ��������˼�룬��ʱ���ŵ�������ĵ¹��ڿ�ҽ�����С��ֲ���Otto Warburg����������ʹ���ڳ�����������㹻�������幦�ܣ���ϸ��Ҳ���Ը����ʷ��������ǣ�1���������Ժ�ϸ��ѡ��ʹ��Ч�ʽϵ͵ķ���;��������Ч�ʽϸߵĺ�����ԭ��һֱ�Ǹ��ա��������ţ������Ѿ������������ţ�ֻ��Ҫ˵�����ˡ�������Ϊ������Ч�ʲ���ܴ���������������������о�����Դ�����ء��෴��������Ϊ��������뷢������IJ����йأ�2����������Ϊ�ø����������ᣬ��ͨ��ʵ�������1�������방֢��Ϯ������أ�3��4����2���к�����Է�ֹ��Ϯ��5-10����3���̼�������Դٽ����֣����أ����У�����ˣ�A�����Ͳ����ᣬB��������������������İ�ϸ������Ӧ�Ժʹ���ʣ�C�����͵İ�֢���п��ܳɹ������������Ǽ��İ�֢��ռ������λ��11-14����
��
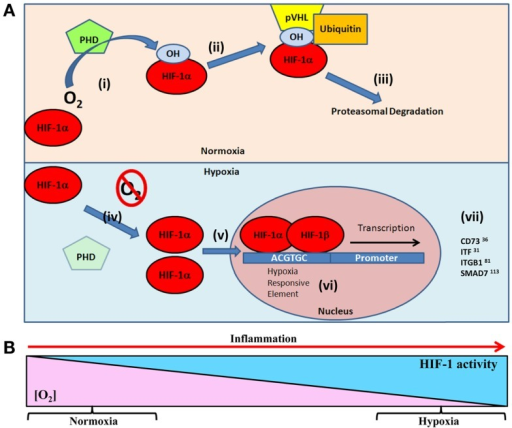
The HIF-1 pathway. Oxygen-sensing prolyl hydroxylase domain enzymes (PHDs) target hypoxia-inducible factor (HIF)-�� subunits for proteasomal degradation in normoxia through hydroxylation.
The HIF-1 pathway. In normoxia, the oxygen-sensing hydroxylases PHD1, PHD2, PHD3 and FIH hydroxylate HIF-1 �� at proline 402 and 564 and at asparagine 803. The prolyl hydroxylations (shown in green) lead to poly-ubiquitination and degradation of HIF-1 �� , while the asparaginyl hydroxylation (shown in red) blocks the recruitment of the co-activators p300 and CBP [CREB (cAMP-response-element-binding protein)-binding protein], inhibiting the transactivation function of HIF-1 ��. In hypoxia the hydroxylases are inhibited, HIF-1 �� escapes the hydroxylations and therefore its degradation and inactivation, translocates into the nucleus, and switches on gene expression.
��
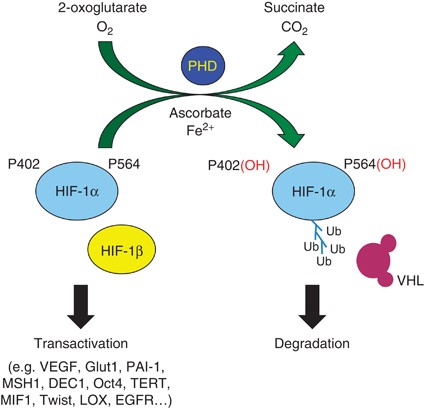
Similar to collagen prolyl-4-hydroxylase ([C-P4H]; EC 1.14.11.2), PHDs require molecular oxygen and 2-oxoglutarate as cosubstrates, as well as ferrous iron and probably l-ascorbic acid (vitamin C) as cofactors for enzymatic activity. 13 K m values of PHDs for oxygen are strikingly higher than those of other prolyl-4-hydroxylases. 13 The relatively low oxygen affinity is essential for effective oxygen ����
��
F1: (A) Oxygen-dependent regulation of HIF-1�� targets in epithelial restitution. Under normal oxygen tensions (normoxia) (i) prolyl hydroxylase (PHD) enzymes hydroxylate the HIF-1�� subunit resident in the cellular cytoplasm (26). Hydroxylated HIF-1�� facilitates, (ii) the binding of von Hippel�CLindau protein (pVHL) and subsequent recruitment of the ubiquitin ligase complex, (iii) targeting HIF-1�� for 26S proteasomal degradation (28). Under conditions of reduced oxygen (hypoxia) (iv) the lack of oxygen substrate for PHD prevents hydroxylation of HIF-1�� leading to (v) cytoplasmic accumulation and translocation to the cell nucleus (29). (vi) HIF-1�� dimerizes with HIF-1�� and binds to hypoxia responsive elements (5��-ACGTGC-3��) in the promoter of target genes (21, 30). (vii) This leads to transcription of HIF target genes involved in epithelial restitution. (B) As tissue oxygen levels gradually decline, HIF stabilization increases. This results in graded HIF stabilization during progressive hypoxia (31), such as the progression of inflammation.
https://openi.nlm.nih.gov/detailedresult.php?img=PMC3769679_fimmu-04-00272-g001&req=4
��
Von Hippel Lindau Protein - an overview | ScienceDirect Topics
https://www.sciencedirect.com/topics/medicine-and...
Von Hippel Lindau Protein. VHL protein (pVHL) encoded by the Vhl gene was further revealed as a component of a ubiquitin ligase complex (Maxwell et al., 1999) required for the specific degradation of hypoxia-inducible factor (HIF) discovered at the same period (Semenza and Wang, 1992).��
PHD2 in tumour angiogenesis
D A Chan & A J Giaccia
British Journal of Cancer volume 103, pages1�C5(2010)Cite this article
Originally identified as the enzymes responsible for catalysing the oxidation of specific, conserved proline residues within hypoxia-inducible factor-1�� (HIF-1��), the additional roles for the prolyl hydroxylase domain (PHD) proteins have remained elusive. Of the four identified PHD enzymes, PHD2 is considered to be the key oxygen sensor, as knockdown of PHD2 results in elevated HIF protein. Several recent studies have highlighted the importance of PHD2 in tumourigenesis. However, there is conflicting evidence as to the exact role of PHD2 in tumour angiogenesis. The divergence seems to be because of the contribution of stromal-derived PHD2, and in particular the involvement of endothelial cells, vs tumour-derived PHD2.PHD2 in tumour angiogenesis | British Journal of Cancer
https://www.nature.com/articles/6605682��
RED CELLS, IRON, AND ERYTHROPOIESIS| MAY 19, 2011
Vitamin C is dispensable for oxygen sensing in vivo
Abstract
Prolyl-4-hydroxylation is necessary for proper structural assembly of collagens and oxygen-dependent protein stability of hypoxia-inducible transcription factors (HIFs). In vitro function of HIF prolyl-4-hydroxylase domain (PHD) enzymes requires oxygen and 2-oxoglutarate as cosubstrates with iron(II) and vitamin C serving as cofactors. Although vitamin C deficiency is known to cause the collagen-disassembly disease scurvy, it is unclear whether cellular oxygen sensing is similarly affected. Here, we report that vitamin C�Cdeprived Gulo−/− knockout mice show normal HIF-dependent gene expression. The systemic response of Gulo−/− animals to inspiratory hypoxia, as measured by plasma erythropoietin levels, was similar to that of animals supplemented with vitamin C. Hypoxic HIF induction was also essentially normal under serum- and vitamin C�Cfree cell-culture conditions, suggesting that vitamin C is not required for oxygen sensing in vivo. Glutathione was found to fully substitute for vitamin C requirement of all 3 PHD isoforms in vitro. Consistently, glutathione also reduced HIF-1�� protein levels, transactivation activity, and endogenous target gene expression in cells exposed to CoCl2. A Cys201Ser mutation in PHD2 increased basal hydroxylation rates and conferred resistance to oxidative damage in vitro, suggesting that this surface-accessible PHD2 cysteine residue is a target of antioxidative protection by vitamin C and glutathione.
Topics:ascorbic acid, enzymes, hydroxylation, hypoxia, oxygen, cell culture techniques, cysteine, protein isoforms, alpha ketoglutarate, iron
Vitamin C is dispensable for oxygen sensing in vivo ...
https://ashpublications.org/blood/article/117/20/...Emerging novel functions of the oxygen-sensing prolyl hydroxylase domain enzymes
Oxygen-sensing prolyl hydroxylase domain enzymes (PHDs) target hypoxia-inducible factor (HIF)-�� subunits for proteasomal degradation in normoxia through hydroxylation. Recently, novel mechanisms of PHD activation and function have been unveiled. Interestingly, PHD3 can unexpectedly amplify HIF signaling through hydroxylation of the glycolytic enzyme pyruvate kinase (PK) muscle isoform 2 (PKM2). Recent studies have also yielded insight into HIF-independent PHD functions, including the control of ��-amino-3-hydroxy-5-methyl-4-isoxazolepropionic acid (AMPA) receptor trafficking in synaptic transmission and the activation of transient receptor potential cation channel member A1 (TRPA1) ion channels by oxygen levels in sensory nerves. Finally, PHD activation has been shown to involve the iron chaperoning function of poly(rC) binding protein (PCBP)1 and the ( R)-enantiomer of 2-hydroxyglutarate (2-HG). The intersection of these regulatory pathways and interactions highlight the complexity of PHD regulation and function.Emerging novel functions of the oxygen-sensing prolyl hydroxylase domain enzymes: Trends in Biochemical Sciences
https://www.cell.com/trends/biochemical-sciences/fulltext/S0968-0004(12)00159-4��
����ЧӦ����Դ���ս� Origin and Termination of Warburg Effct
��
�ֱ�ЧӦ����Դ
��Ŀ�ܽ
���ϸ����������������ATP���������ƣ�������������ǽͽⷢ�͡�ͨ��·��˹����˹�£�Louis Pasteur���Ŀ������о���������Ϊֻ��������������֧�ֺ���������£�����Ч�ʲŻή�͡�ֱ����Լ100��ǰ����Ȼ��������˼�룬��ʱ���ŵ�������ĵ¹��ڿ�ҽ�����С��ֲ���Otto Warburg����������ʹ���ڳ�����������㹻�������幦�ܣ���ϸ��Ҳ���Ը����ʷ��������ǣ�1���������Ժ�ϸ��ѡ��ʹ��Ч�ʽϵ͵ķ���;��������Ч�ʽϸߵĺ�����ԭ��һֱ�Ǹ��ա��������ţ������Ѿ������������ţ�ֻ��Ҫ˵�����ˡ�������Ϊ������Ч�ʲ���ܴ���������������������о�����Դ�����ء��෴��������Ϊ��������뷢������IJ����йأ�2����������Ϊ�ø����������ᣬ��ͨ��ʵ�������1�������방֢��Ϯ������أ�3��4����2���к�����Է�ֹ��Ϯ��5-10����3���̼�������Դٽ����֣����أ����У�����ˣ�A�����Ͳ����ᣬB��������������������İ�ϸ������Ӧ�Ժʹ���ʣ�C�����͵İ�֢���п��ܳɹ������������Ǽ��İ�֢��ռ������λ��11-14����
��
Origin of the Warburg Effect
Project Summary:
Eukaryotic cells have two mechanisms of energy (ATP) production: mitochondrial respiration and glycolytic fermentation. Through the groundbreaking work of Louis Pasteur, it was thought that the less efficient fermentation would ensue only if there was insufficient oxygen to support respiration. This was the predominant thought until about 100 years ago, when the Nobel Prize-winning German Physician, Otto Warburg showed that cancer cells ferment glucose at a high rate, even in the presence of adequate oxygen and sufficient mitochondrial function (1). The reasons that cancer cells choose to use the less efficient fermentative pathway over the more efficient respiration have remained a mystery ever since. We believe that we have solved this mystery, and only need to convince others. We have argued that as the efficiencies are so different, this has nothing to do with energy production, where most have been focusing their time. Instead, we argue, that it must have to do with the production of a by-product of fermentation (2). We believe that this byproduct is lactic acid, and have shown through experiments that: 1) acid production is associated with increased cancer invasion (3, 4), 2) that neutralization of acid can prevent invasion (5-10), and 3) that stimulation of acid production can promote invasion (Russell, in prep). Hence, A) fermentation produces acid, B) acid production improves the fitness and survival of cancer cells that do this, and C) cancers that ferment are more likely to succeed and be predominant in those that we detect (11-14).https://lab.moffitt.org/gillies/research/tumor-ph/origin-of-the-warburg-effect/
A unifying theory of carcinogenesis, and why targeted therapy doesn��t work - ScienceDirect
https://www.sciencedirect.com/science/article/abs/pii/S0720048X12700189A unifying theory of carcinogenesis, and why targeted therapy doesn't work. - PubMed - NCBI
https://www.ncbi.nlm.nih.gov/pubmed/23083599
References:
Warburg O, Posener K. Uber den stoffwechsel der carcinomzelle. Bioichem Z 1924;152:309-44.
Gillies RJ, Robey I, Gatenby RA. Causes and consequences of increased glucose metabolism of cancers. J Nucl Med 2008;49 Suppl 2:24S-42S.
Estrella V, Chen T, Lloyd M, Wojtkowiak J, Cornnell HH, Ibrahim-Hashim A, et al. Acidity generated by the tumor microenvironment drives local invasion. Cancer research 2013;73(5):1524-35.
Gatenby RA, Gawlinski ET, Gmitro AF, Kaylor B, Gillies RJ. Acid-mediated tumor invasion: a multidisciplinary study. Cancer research 2006;66(10):5216-23.
Ibrahim Hashim A, Cornnell HH, Coelho Ribeiro Mde L, Abrahams D, Cunningham J, Lloyd M, et al. Reduction of metastasis using a non-volatile buffer. Clin Exp Metastasis 2011;28(8):841-9.
Ibrahim-Hashim A, Abrahams D, Enriquez-Navas PM, Luddy K, Gatenby RA, Gillies RJ. Tris-base buffer: a promising new inhibitor for cancer progression and metastasis. Cancer Med 2017.
Ibrahim-Hashim A, Cornnell HH, Abrahams D, Lloyd M, Bui M, Gillies RJ, et al. Systemic buffers inhibit carcinogenesis in TRAMP mice. J Urol 2012;188(2):624-31.
Ibrahim-Hashim A, Robertson-Tessi M, Enriquez-Navas PM, Damaghi M, Balagurunathan Y, Wojtkowiak JW, et al. Defining Cancer Subpopulations by Adaptive Strategies Rather Than Molecular Properties Provides Novel Insights into Intratumoral Evolution. Cancer research 2017;77(9):2242-54.
Ribeiro MD, Silva AS, Bailey KM, Kumar NB, Sellers TA, Gatenby RA, et al. Buffer Therapy for Cancer. Journal of nutrition & food sciences 2012;2:6.
Robey IF, Baggett BK, Kirkpatrick ND, Roe DJ, Dosescu J, Sloane BF, et al. Bicarbonate increases tumor pH and inhibits spontaneous metastases. Cancer research 2009;69(6):2260-8.
Gatenby RA, Gillies RJ. Why do cancers have high aerobic glycolysis? Nat Rev Cancer 2004;4(11):891-9.
Gatenby RA, Gillies RJ. A microenvironmental model of carcinogenesis. Nat Rev Cancer 2008;8(1):56-61.
Gatenby RA, Gillies RJ, Brown JS. Evolutionary dynamics of cancer prevention. Nat Rev Cancer 2010;10(8):526-7.
Gillies RJ, Verduzco D, Gatenby RA. Evolutionary dynamics of carcinogenesis and why targeted therapy does not work. Nat Rev Cancer 2012;12(7):487-93.��
ͨ������Ӧ���Զ��Ƿ������ʶ��尩֢��Ⱥ��Ϊ�����ڽ����ṩ���µļ���
�����������ڽ�����intrarumoral evolution)��ͬһ������ͬ����İ�ϸ��֮��ķ��ӱ����к����ԣ����ǽ����Ŵ����ݾ����˽��ѡ����(environmental selective force)�Ϳ���DZ�ڵĴ���Ķ���ѧ(Darwinian dynamics)��ϸ��������Ӧ�ԡ��������Է������֢��TRAMP��PTENС���ǰ���ٰ���KPCС������ٰ����У����Ǽ�����������Ⱥ�����Ǿ��ж��ص� ��̬����������Ӧ�Բ��ԣ�niche construction adaptive strategies)�������������б����ȶ�����i��ͨ���ϵ� �����ǽͽ����Ӳ������Ϯ��ϸ�� ��ii��Ѫ�����ɺʹ�л�ӽ������ķ�������ϸ������TRAMPǰ���ٰ����о�����Щ��Ⱥ�Ĵ���������(Darwinian interactions)�������ģ������������Բ��ᣨC2��ϸ��ͨ���ٽ����벢�������߷�Ӧ�Ĺ�Ч������ڷ�������Ѫ�����ɣ�C3��ϸ�������� �������ơ�δ�����Ƶ�������������֯��ѧ����֤ʵ��C2ϸ�����DZ�C3ϸ���ḻ��Ȼ����������������Ч�ʵͣ��������ǽͽ⣩��������Ӧ���Ի�������Դ�ݽߣ�C2��Ӧ�Բ��Ա��Ͳ����˿ɹ۵ijɱ�����ѧģ�ͷ���Ԥ�⣬����ϸ����pH��pHe����С�Ŷ����ܻᷴתC2���Եijɱ�/����ȣ���ѡ��C3ϸ���������ڣ���4�ܴ��TRAMPС�������ˮ������200 mmol / L NaHCO3�ɽ�ǰ������pHe����0.2����λ�����ٽ���������C3ϸ������ֳ�������Ա������ڵ����ڣ���˲��ᷢ��ԭ����֢�����ѽ����������У�0.2 pHe�����ӻ�����C3ϸ���ı����������ż���ԭ���Ժ�ת������������������ʵ���Ե������������У���MCF7��MDA-MB-231���ٰ�ϸ����ע��SCIDС�������֬�����С� C2��MDA-MB-231ϸ����δ�����ƵĶ�����ռ������λ������������pHe����ʱ��ѡ����C3��MCF7ϸ��������������������������ԣ����ǵ�����֧�ֶԻ���ѡ�����Ͱ�ϸ����Ӧ���Ե������ڴ��������õ���ѧ��ģ����Щģ������ͨ��ʩ�ӽ�С��ѡ���Ե������������������������Խ�С��;������֢�о��� 77��9��; 2242�C54�� ©2017 AACR��
��Ҫ����
ͨ������Ӧ�Բ��Զ����Ƿ�֧��¡����ģ����ʹ�õķ���������������������Ⱥ��������ѧ��ʽʶ�����ϸ���ͻ���������á��ڳ���˽�DZ�ڵ���̬������������£��������ø��ӵĶ�̬ϵͳ�Ŵ�С�Ŷ������ƣ�ͨ��Ӧ����Խ�С�������Ŷ����������������������������ơ���
A������ͼ�����ڲ�ͬ������ÿ��ϸ��ϵ�ͻ���MDA-MB-231��MCF7��1��1���Ĵ�����������H��Eͼ����ͼ����H��E����ͬ������������Ƭ��ERȾɫ�� B���ڸ�ʵ����ʹ�õ�����������ER����ķ�������ע�⣬��̼������400 mmol / L��������Щ��������MDA-MB-231��MCF7�Ļ���1��1��ɣ����е�ER����Ҫ������ˮ�еĸ���P = 0.0001���� C����ʵ����ʹ�õ�����������MRI������ݡ����ݱ�ʾΪ����������������ע��������ı仯��������ʾ��ƽ��ֵ��SEM��ʹ����βѧ��t����������ͳ��ѧ�����ԡ�
��
��̬λ����������Բ���ģ�͡����ǵļ����ǣ�������������ͬ��ϸ����Ⱥ��ɣ��߶��ǽͽ�IJ���ϸ������ϸ�����ͷ��ǽͽ�ķDz���ϸ������ϸ���������ǵ�ģ��Ԥ�⣬pHe��С�Ŷ����ܻ��յ���Ⱥ��䣬�Ӷ������ڷDz��ᣬ����Ϯ��֢��Ⱥ�� PIN��ǰ������Ƥ�����䡣Model for manipulation of niche construction evolutionary strategy. Our hypotheses is that tumors consist of two distinct subpopulations of cells, highly glycolytic, acid-producing cells (red cells), and nonglycolytic, non�Cacid-producing cells (blue cells). Our model predicts that small perturbations in pHe could induce a population phase transition favoring the non�Cacid-producing, noninvasive cancer populations. PIN, prostate intraepithelial neoplasia.
��
����
���ڵ�һЩ�о����������֢�IJ��Ϸ�չ���������Ŵ�ѧ�϶���Ŵ��ϲ�ͬ����Ⱥ��1��2�������ǣ�����ע������Ŵ�ѧ���������ṩ�Ի���ѡ��ѹ����ϸ����Ӧ���Ե������˽⣬�������ǿ��ƴ���Ķ���ѧ����ԭ���ЧӦ��ϵ��3������������ǽ����ڽ�����Ϊ��Ⱥ֮��Ķ�̬����ã�����������������Ծ���������ͨ����Ӧ�����Լ���Щ�������������Ե�����������塣
���ǽ������һ�������⣺��i�����ǿ��Զ��岻ͬ��֢֮�䳣������Ӧ�Բ����� ��ii��֧����Ⱥ�������ھ����Ľ�������ѧ��ʲô�� ��iii����Щ��ϸ���ͷ��ӳ߶��ϵĴ������������Ӱ��������������֯�߶ȱ仯��
����ͨ���о���TRAMP��PTEN��KPC����������л�õ�������Ⱥ�������һ�����⣬��Щ���ᆳ�����̸�����γ���ԭ����֢��6-8������ijЩ����£�PTEN��TRAMP������ȺԴ����ͬ����������ÿ�������У����Ƿ��������������Ⱥ���в�ͬ����Ӧ�Բ��ԣ��������������б����ȶ���
��һ�������Ա��ͣ���ʹ������������£�Ҳ��ͨ���ϵ�����������;�������������ᡣ
ά�ֽ��������������Ǵ�л�ķ������ԣ�Ѫ�������ԣ����˶��Ա��͡�
������С��������9���Լ��ٴ����ٰ���10�����᳦����11����Ƥ������12���Ͷ����Խ���ĸϸ������13���У��Ѿ���������Ϯ�Ժ�Ѫ��������Ⱥ���档����������ձ�����
����ͨ��Ӧ�ö�߶���ѧģ�ͣ������ģ��ο�����4��5��14������������Ӧ����֮�����̬�����������Ӷ�����ڶ������⡣ģ�ͷ���������������ǽͽ���Ⱥͨ��������������ڴ�������������и�Ϊ�ḻ�����ǣ�ģ�ͷ��滹��������������Ա��͵����ֳɱ�/�������ɱ���С�����ӻ�������½�����ת�������ĵĶ�̬���ܻ���ת���Ӷ�������������Ⱥ�����½���
��TRAMPС��ģ���в�������ЩԤ�⣬��ģ����Լ12����ʱ��չΪԭ����ǰ���ٰ�������52����������ԭ���Ժ�ת���Բ�������Ⱥ��IHC֤ʵ��ģ��Ԥ�⣬�������ԣ����ᣬ�ǽͽ���ͣ���ΪC2������ḻ����Ⱥ��Ȼ�����������ڵ��ܣ���ԭλ��ǰ������Ƥ���������䣩ʱ����4����ʱ������ˮ��15��16��������200 mmol / L NaHCO3���Ӷ�����������ϸ����pH��pHe��0.2����λ��ʬ��ʱ������������ŵ���Ⱥת�ƣ������ڷ������ԣ�Ѫ�����ɣ������ᣨ��ΪC3�����͡�Ҫʹ�ѽ���������pHe�������ƣ���Ҫ��ˮ������400 mmol / L NaHCO3���������ʼ�ʱ��C3��������Щ��������Ҫ��Ⱥ��Ϊ�˽�����������⣬���ǹ۲쵽�ڽ���4�����ƵĶ����У�����C3����û�д�����Ĥ���������������ȫ���ڵ����ڣ��Ӷ���ֹ����Ϯ��ԭ���������ķ�չ��ͬ��������ȷ�������Ķ����У�ԭ����ת�����������Լ��١�
���ǽ�һ���о���ʵ���������е�����2��3����ʵ������������Ϯ���������ٰ�ϸ��ϵMDA-MB-231�ͷ���Ϯ���������ٰ�ϸ��ϵMCF7���ע�����������֬���湹�ɵġ������⣬MDA-MB-231ϸ�����ֳ����и�ˮƽ�˶��Ե�C2�����ͣ��������ϵ������ǽͽ�Ͳ��ᡣ MCF7ϸ����C3���������Ǵ�л�ӽ��������˶�����Ϯˮƽ�ϵ͡������ڣ�MCF7ϸ�����и߶�Ѫ���������ã�17����������C2 / C3���ַ���MDA-MB-231ϸ����δ���ƶ����е���Ҫ��Ⱥ�����ǣ�����NaHCO3���ӵ�����ˮ��ʱ��MCF7��Ⱥ������ӣ�MDA-MB-231��Ⱥ���٣������������������Լ��������Ϻͷ���
ϸ������
ʹ�û���ATCC��ATCC��CRL-2731��-2733����С��TRAMP-C2��TRAMP-C3ϸ��ϵ����ʵ�顣����ϸ��ϵ���ڲ�����10��FBS��1����ù��/��ù�أ�100 nmol / L DHEA��0.005 mg / mL�ȵ��ص�DMEM����������������ATCC��ATCC��CRL-3033��-3031�����MCF7ϸ����MDA-MB-231��PTEN-P8��PTEN-CaP8ϸ��ϵ���������ڲ����RPMI������1640��Life Technologies Gibco��11875-093�����ڱ�ϸ������������ʹ��10��FBS��HyCloneʵ���ң��� UN-KPC-960��UN-KPC-961����ϸ��ϵͨ��MTA��Batra��ʿ���ڲ���˹���ݴ�ѧҽѧ���ģ��ڲ���˹���ݰ������У���ã��������ں���������FBS��1-�Ȱ�������200 mmol / L����DMEM�С� L����100���DZ��谱���ᣨ100 mmol / L����̼�����ƣ�HEPES����Һ�����ù�أ�50 mg / mL������ù��/��ù�أ�100��g/ mL���������е��ά����37��C��5��CO2�¡����в������������������֯�������н��С�
���е�ؾ��ڹ�����6������ʹ�ã�����ͨ���̴����ظ���STR������������������֤������ϸ������2012����2015��֮���á���MDA-MB-231�⣬����ϸ��������16�����µĴ���������ϸ������֧ԭ�塣�����6�����ڣ���MCF7ϸ��MDA-MB-231�⣬����ϸ������ʹ�á� MCF7ϸ��MDA-MB-231��ͨ��Moffitt��֢���ģ�Tampa��FL���ķ�������ѧ�����е�STR������֤��
�����ֳ������
��ǰ�Ѿ�������TRAMPС��ķ�ֳ��18���������֮��ʹ�ñ������ת����C587BL / 6����С��Ҳ����The Jackson Laboratory���ӽ���TRAMPת������Ӻϴ���С��Ҳ���Խܿ�ѷʵ���ң�Jackson Laboratory���������˷�ֳȺ�壬���Ժ�������˶���������͡������������������о�Ժ��ʵ�鶯��Ļ�����ʹ��ָ�ϡ��͵��ػ������ﻤ����ʹ��ίԱ���ָ��ԭ�����������ڸɾ�����ʩ��USF Vivarium��λ��Ī���ذ�֢�о����ģ�������õ�4�����TRAMPС�������Ϊ���Զ�����������顣��̼�����ƣ�200��400 mmol / L���ܽ�������ˮ�У�����4�����10���俪ʼ��TRAMPС�����á����С���ˮ���ĺ����ز���������������ˮ��С���գ����бȽϡ�������ת����С����Ϊ���Զ��ա����ö����������������Ӧʵ���ͼ���С�
��һ��30 nu / nuС��Harlan��ע�䵽����֬�����У����к���1��107 MDA-MB-231ϸ����1��107 MCF7ϸ����������ǰ��ϸ��ϵ��5��106��ɵĻ�����ϸ��ע��ǰһ�ܣ����Ƽ��س�����0.72mg���ͷţ����������о���ֲ������С���С�ע�����������С�������Ϊ�������δ�����飨�����飩��������n = 4��������n = 6����������С�������ˮ��̼�����κ���Ϊ400 mmol / L��������С����ʹ�ó�������ˮ��ʹ��MRI T2���������ز��������У�TE / TR = 60/900 ms��ÿ�ܲ���һ������������������ڷֱ���Ϊ273��m����Ƭ���Ϊ1.5 mm��ʵ�鿪ʼ���ܺ��ռ�����������ľ������죨H��E���ʹƼ������壨ER���ı������Ⱦɫ����IHC��Ƭ�����˷�������������֯ѧ������������������ϸ�����ữ����
TRAMP-C2��C3��MCF7��MDA-MB-231��PTEN-P8��PTEN-CaP8��KPC 960��KPC 961ϸ��ϵ�������˵�ʵʱ���������ģ�OCR����ϸ�����ữ�ʣ�ECAR��ʹ��Seahorseϸ����ͨ����XF-96�������ǣ�Seahorse Bioscience��ȷ��ԭ��ǰ������Ƥϸ����PCS���� XF-96ʵʱ��������ϸ���Ϸ����������������������ӵ�Ũ�ȡ��ڴ��ڻ���2 g / L d-�����ǵ�����£���XF�װ��н��ֵ�ϸ������2Сʱ��Ȼ���ٽ���OCR��ECAR������ʹ�ñ�BCA���ײⶨ��ȷ��ÿ���ĵ���Ũ�ȡ���OCR��ECARֵ����Ϊmg /�����ʣ�������Ϊƽ��ֵ��SD���ڷ������֮ǰδ������Ʒ������Seahorse�����У����κθ�����һ�죬ÿ�������������Ŀף���Ʒ�ظ�����ÿ��������ÿ�ֲ����ظ�3��5�Σ������ظ��������Ҷ������ж�η���������ѧ�ظ���������PTEN-P8��PTEN-CaP8ϸ����ÿ������ÿ������ÿ��������������ѧ������ⶨ���ĸ������ظ������У�ʹ�����ֲ�ͬŨ�ȵĹ�ù����ȷ���ﵽ�����Ч������1��2��mol/ L�������ּ�����������ͬ�Ľ������˽�1��mol/ L��ù�����ں���������ѧ���ơ�����KPC 960��KPC961���ֱ�ⶨ��1������ѧ��Ʒ��11����Ʒ��8����Ʒ�Լ�4�������ظ���Ʒ������MCF7��MDA-MB-231��TRAMP C2��TRAMP C3��PCS��ÿ�βⶨÿ��ϸ��ϵʹ����������ѧ��8����Ʒ��3-4�������ظ���Ʒ��ͳ�Ʒ����ڼ����˹�ֲ�������£�����δ���t�����WelchУ������
Ѫ�Ʋ���
ʹ�ô�CG8 +ҩͲ��iSTAT��Яʽ�ٴ������ǣ�Abaxis�����Ѫ��Ũ�ȡ���С���������л�ȡѪ����Լ200��L�����������ҩͲ�������������̵Ĺ���¼������
����MMPSense 680���ԵIJ���
����Tap��TRAMPС���ڵ�4�ܺ͵�10�ܣ�ÿ������n = 6����32����ʱ����400 mmol / L NaHCO3��������ǰ��ʮ��Сʱ�����ɼ����ӫ��̽��MMPSense 680��PerkinElmer������ע���С��Ȼ��ʹ��FMT2500��PerkinElmer���ϲ����ϵͳ��С��������ڳ���ʹ���ڱ�Ը���Ȥ���������������һ����
����PCR
ʹ�ô���SYBR Green��iScript Real-Rime PCR Kit��Bio-Rad��170-8893������7900HT����ʵʱϵͳ��Life Technologies Applied Biosystems���Ͻ�������qRT-PCR�� GAPDH���������ڲ����ա�ÿ20��L��Ӧʹ��mRNA��100 ng���� TRIzol��Life Technologies Invitrogen�����������̵�˵����������RNA������ʹ��RNeasy Mini Kit��Qiagen��������pH 7.4��TRAMP-C2�͵�pH��6.7��������ϸ�������з���RNA��
MMP-2��MMP-9�����ﹺ��Srikumar Chellepan��H��Lee Moffitt��֢���ĺ��о��������������а����ڲ�����Ϻͷ����С�
��֯ѧ��ͼ�����
ʬ��ʱ���ռ���/���࣬�����������ֳϵͳ��������֯�����������ʯ���У����4��5��m����֯��Ƭ�����ز�Ƭ��H��EȾɫ��Ⱦɫ�����ɲ���ѧ�Ҷ�������֯�Ĵ��ڽ��зּ���ʹ�ô���20x / 0.8NA�ᄉ��200x����Aperio ScanScope XTͨ��Basler������������ÿ����2���ӵ��ٶ�ɨ����֯ѧ��Ƭ�� Aperio�����ؼ���v9.0�㷨[����������ֵ��ɫ��ֵ= 0.1��ɫ�����= 0.5;��ɫ���Ͷ���ֵ= 0.04; IWP���ߣ�= 220; Iwp���ͣ�= Ip���ߣ�= 175; Ip���ͣ�= Isp���ߣ�= 100 Isp���ͣ�= 0]�����ڷָ����ǿ�ȵ�����Ⱦɫ�������㷨Ӧ�����������ֺ���ͼ����ȷ��������������������־��Ⱦɫ�İٷֱȡ�����
���¡�ÿ�С��GLUT-1���幺��Millipore��07-1401��1��800��Ũ��ʹ�ã�����CD31��Ӧ���ÿ��幺��Abcam��ab28364;��1��200��Ũ��ʹ�ã�;��SMA��Ӧ���ÿ��幺��Abcam��ab32575��ʹ�õ�Ũ��Ϊ1��250������VEGF��Ӧ���ÿ��幺��Abcam��ab46154����1��1,500��Ũ��ʹ�ã�����ER��Ӧ���ÿ��幺��Abcam��ab32063����1��250��Ũ��ʹ�ã������������̵Ĺ�̣�ʹ��Ventana Discovery XT�Զ���ϵͳ��Ventana Medical Systems����ר���Լ��Բ�Ƭ����Ⱦɫ��
ϸ��Ǩ�ƺ���Ϯ������ⶨ
ʹ��xCELLigenceʵʱϸ�������ǣ�RTCA��ACEA Biosciences���Ƚ���C2-��C3-TRAMPϸ��ϵ�������˶��Ժ���Ϯ���Լ�MDA-MB-231��MCF7�������˶��ԡ�Ϊ�˽���Ǩ�Ʋⶨ����ϸ����2��104��ϸ��/��CIM16ƽ������ں�����Ѫ������������ǻ���У�����ǻ��װ����Ѫ�������������Զ��գ�����10��FBS����������ͨ������ϸ���������迹��ϸ��ָ����ʵʱ���������ǻ��֮��Ĺ������±���Ǩ�Ƶ�ϸ��������Ϊ�˽�����Ϯ�ⶨ������ǻ�ҵĹ�������ԤͿ��10����Cultrex����Ĥ��ȡ����ϸ��ָ���ı仯��ֱ��Ǩ��24Сʱ����Ϯ72Сʱ��Ǩ�ƺ���Ϯ���飨xCELLigence��������������ѧ�ظ���ÿ������ÿ�������ÿ��ϸ��ϵn = 8��
���ݴ���
ʹ��Microsoft Excel��GraphPad Prism�������ݴ���������ͳ�������ԣ�P��0.05����
ͳ�Ʒ���
������βδ��Ե�Student t����ȷ��ͳ��ѧ�����ԡ�С��0.05��Pֵ����Ϊ����ͳ��ѧ���������ָʾ�������������������һ�ַDz���ͳ����������ڵȼ��ļ���������ƣ�����Ǩ�ƺ����ּ�⡣��
���
��������������Ⱥ��C2��C3��������
�Ӳ�ͬ�Ŀ�¡�н�����TRAMP-C3��TRAMP-C2ϸ��ϵ����Щ��¡�Ǵ�32������TRAMPС�������з�������ģ�6��������ϸ��ϵ��������������ֳ�������ȶ��ı��͡������ڣ�TRAMP-C2ϵ�γ���Ϯ����������TRAMP-C3���γɡ�Ϊ�˼�����ǵĴ�л�ף�������ϸ��ϵ�����������Ǽ���2Сʱ��Ȼ��ʹ��Seahorseϸ����ͨ����XF�������ǽ��з�������ͼ1A��ʾ����TRAMP-C3��ȣ�TRAMP-C2ϸ���������ţ�P = 0.027���������Ǵ̼��ữ���ʣ����������ǽͽ����ʸ��ߡ����⣬�ڻ��������£�TRAMP-C3ϸ����ʾ���ӽ������ǽͽ�������������ͬ�����£�TRAMP-C2ϸ��ȴԶδ�ﵽ������ C2ϸ��ϵ�Ļ���OCRҲ�������ţ�P = 0.0054��������C3ϸ����ͼ1B�������������ͼ1A��B�����ݱ���C2ϸ����ATPת���ʸ��ߣ����Ҷ��ǽͽⷢ�͵������Ը��ߡ���TRAMP-C2ϸ����ȣ������������ż����FCCP���Բ�������DZ��OCR����Ϊ���Ӵ��䶯��ѧ�����ȣ�����֤��TRAMP-C3�е��������������Ÿ��ߣ�P = 0.0082������
ͼ1��
����ͼƬ���±�ǩ�д�����PowerPoint
ͼ1��
A�CD������TRAMP-C2�ͷ�����TRAMP-C3ϸ��ϵ����������� A��ʹ��Seahorse XFe-96������ʵʱ����ECAR�Ĵ�лͨ����������C3ϸ��ϵ��ȣ�C2ϸ�����ֳ����ӵ��ǽͽ⡣ *��P �� 0.0274���ǽͽ�������C2ϸ���нϸߡ� **��P �� 0.001�� B������ϸ��ϵ�Ļ���OCRû�в�ͬ�� C3ϸ���ĺ�������������ߣ�������������ߡ� **��P �� 0.0082�� C�������˶��ԣ���ͨ��������ϸ��ϵ�е�Ǩ��������迹������������xCELLigenceʵʱϸ��������������¼��C2ϸ�����и�Ǩ���ԣ�����C3ϵ����� ***��P �� 0.0007�� D��ͨ���迹���Ӳ�����C2-��C3-ϸ��֮�����Ϯ�ԱȽϣ���transwellǨ�Ʒ�����C2ϸ��������Ϯ�ԡ� **��P �� 0.0015��������Mann-Whitneyͳ�Ƽ��飬��������ʱ�������������Բ�ͬ����Ⱥ��Ǩ�ƺ����־���һ��Ϊ��ֳ���ʡ���
����ǽͽ������ͼ1A��B������Щ�������C3ϵ��Ҫͨ���������ã���������л�����������������͵�����Ӧ�Ա���C2ϸ������и߶ȵ��ǽͽ����á���������C2 TRAMPϸ��ϵ������ǰ������Ƥϸ��ϵ��PCS����ȵĴ�л�ס���PCS��ȣ�2-DG���C2Ʒϵ��ʾ�����ߵ��ǽͽ�����������ECAR���Ž��ͣ�P <0.0001�������⣬C2ϸ�������и��ߵ�OCR���������л�ʣ���ˣ�������ǰ������Ƥϸ��PCS��ȣ�C2ϸ����ATP��������������ߣ�P <0.0001����������ͼS1A�CS1D���� C2ϸ���нϸߵ��ǽͽ����ʣ���������������ϸ��ATP�����ܸ�������Ĥ�϶�ATP�����ķָ�������ο�����1�������� 16.���ǽͽ����ӵ�ϸ���о������������ǹ۲쵽GLUT-1�ı�����ǵ�IHC���������ͼS2A��S2B����ʾ�����������Ƶ�С��Ķ��Ը��ߵ�TRAMP������֯�У�GLUT-1���ߣ�����̼���������Ƶ�С��Ķ��Գ̶ȸ��͵������У�GLUT-1���Խ��ͣ�P = 0.002�����μ����ģ� �������ǽ�����Щ���֣��Ա������нϸ�GLUT-1ˮƽ�ĸ�����TRAMP����Ҳ���нϸߵ������Ǵ̼�������ʡ�
��ϸ���и����ʵ��ǽͽ�Ͳ���֧�ֿ��٣���Ϯ�Ժ�ת����������19������ˣ�����ʹ����xCELLigence��ǩ��ƽ̨�о�������ϸ��ϵ��Ǩ�ƺ���Ϯ����������IJ��Ϻͷ�������ͼ1C��ʾ���ڴ��ںͲ�����FBS������£�ÿ��ϸ��ϵ��Ǩ���������Ժ����迹��ϸ��ָ������ C2ϸ���������ţ�P = 0.0015���ĸ�Ǩ�����ʣ���û��FBS������½�����Ǩ�����ʣ���C3ϸ�������������¾�û��Ǩ��������ͼ1D��ʾ�˿��Ǩ�Ʋⶨ�����迹�����ӣ�����ϸ������Խ��Matrigel���ϳ�����FBS��Ϊ��ѧ���������²��״������Բ����źš���Ǩ�Ʒ������ƣ���C3��ȣ�C2ϸ��ϵ����Ϯ�����ţ�P = 0.0007����
����������̬λ���̱����Ƿ���������֢�з������ԣ����������Ⱥ������
����̬λ���衱��һ����̬����������������ĸ�����ʹ���ֻ��ѽ������������档���Dz�������������������ְ�ϸ����Ϊ���ṩ�������ķ�ʽ����ֲ�������������ͬʱ����������֯����Ӧ�ԡ������������ھ���������֢�У�FdG PET����������������������ȡ�Ĺ۲��������������������������ڰ�֢�Ĺ�ͬ������ϵͳ���о����а�֢���ͳ����˱�����ķ�Χ�����ǣ�����ȷʵ�����˴�PTEN��Ч��ת����С���з����ǰ������Ƥϸ������ЩС��Ҫô���Ӻ��ӣ�PTEN-P8��Ҫô�Ǵ����ӣ�PTEN-CaP8��ȱʧ��PTEN������ͼS3A��S3B���ο�����7�����Լ���Ƥ����������KrasG12D; Trp53R172H; Pdx1-Cre��KPC��ģ�ͣ�UN-KPC-960��UN-KPC-961��ϸ��ϵ������ͼS4A��S4B;�ο�����8�������ǹ۲쵽��������C2 / C3���Ͷ��ַ���PTEN-P8ϸ���Ƿ������Եģ�UN-KPC-960�Ƿ�ת���Եģ����Ҷ�������������л����������PTEN-CaP8��ת���Ե�UN-KPC-961ϸ���Ǹ߶��°��ġ��ǽͽ⣨�ֱ�ΪP <0.01��P <0.001����������С��������6���Լ��ٴ����ٰ���7�����᳦����8����Ƥ������9���Լ������Խ���ĸϸ������10���У��Ѿ���������Ϯ��Ѫ��������Ⱥ���档��Щ���ݱ�����ͬһ�����ڰ�ϸ���Ĵ�л���Ͷ��ַ��������ձ�������
C3����������TRAMPС���Ѫ����
������ΪC2��ϸ���IJ�����һ�������ṹ����ʽ��������ʹϸ��������Χ����֯�������������Ѫ�ܡ����ǣ�����ע���C3��ϸ��Ҳ���ܲ�����������������������ԣ���������ͨ���ٽ�������Ѫ�ܵ����������������ֳ��ʹ�ö�̬�Ա���ǿMRI�������о���ͼ2A��B�����������������ȣ�̼���������Ƶ���������ҪΪC3�ͣ������ģ��۲쵽���ţ�P <0.0001�����Ӳ��ҹ۲쵽�ռ��ϸ����ȵ�Ѫ����ͼ2C����������������Ľ�һ��IHC������������̼�����δ���������ÿ��λ�����Ѫ���������Ը��ߣ�P = 0.0004����Ѫ��ֱ����С��P = 0.029����ƽ�����������ı�����ߣ�P = 0.04�� ����VEGF�����½���P = 0.03����Ҳ��Ѫ��������һ�£�����ͼS5A�CS5F����
��
ͼ2��
̼�����ζ�TRAMP��ע��Ӱ�졣 A�CC��ʹ��g����̬�Ա���ǿ��DCE��-MRI��������������ϵͳ����ע��ͨ�ԣ���A���Ĵ����200��TRAMPǰ����������״����DCE-MRI�Ĵ�����ͼ����ʾ��mmol / L̼�����λ��š���ʱ��0����ע��֮ǰ���ͣ�ע���4��7��10���ӻ��ͼ��ɫ���ʾǰ�������ź�ǿ�ȵ��������ӡ� B��ʹ��MATLAB���ź�ǿ�ȵij�ʼAUC�������ݷ�������ʾ��200 mmol / L̼�������������нϸߵ�Ѫ������****��P <0.0001���� C����10����ʱ��ǿ��ͳ�Ʒ�������ʾƽ���ź�ǿ�ȡ�SD���Լ���ǿֵ��SD��ֱ��ͼ��ƫб�ȡ�ƽ��ֵ���������ö�����ȣ����Ƶ���ǿ�������ӣ�P = 0.001�������⣬��̼�������飨P = 0.03����ȣ��Ĵ����е���ǿ���طֲ�����̬��P = 0.03�������ǽ������Ϊƫ����߹�עֵ��������ϵͳ��ļ������βѧ��t�������ڼ���ͳ�������ԡ�
�����ھ�����������ѧ����ѧģ��
Ϊ�˼�������Щ������Ⱥ����õĴ���Ķ���ѧ�����ǻ��ڻ��ϸ���Զ�����ʽ��չ�����ǵĶ�߶���ѧģ�ͣ�4��5����������ܵ�������״����ģ�Ͳ����˾���������ϸ�����ͺ�����ѡ�������������������Ǻ����ж����ĸ���ʱ������ã�ͼ3A��B������ģ�͵���ϸ��Ϣ֮ǰ�Ѿ���������4��5��20�������Ǻ���Ԫ����ͼ3A��B������ʽ�ͼ������ָ���Լ����䷽���н�����˵����ģ�ͷ�������������������ͽ���ռ������λ��������Ⱥ���ñ��͵���Ϯ�Զ��ڴ�ԭλ������Ϯ����ת���Լ�ԭ���Ժ�ת������������Ϯ������������Ҫ��ͼ3C�CE����
��
ͼ3��
���Բ�ͬ��ʼʱ��ͼ���̼�����Ƶ����������Ķ�߶���ѧģ�͵Ľ���� A������ϵͳ�����������ж�����ɫ���������ɷ�������ϸ�����ͣ���������ɫ�����ᣬ��ɫ���ǽͽ⣬��ɫ���ǽͽ�����ᣬ�ۺ�ɫ��֮��������ģ�͡� B��ÿ������ϸ�����ص�ϸ��������������ͼ����ʾ������pH��ATP�Ϳռ������������Լ�����ϸ����ֹ����������ֳ�ľ����� C��D�����Ϳռ䣨C���������ռ䣨D��������������������ʾΪt = 200�죺��i�����ڸ���ͼ���̼�����Σ�t = 40�죩�� ��ii�������������� ��iii�����ڣ�t = 150�죩����ͼ����� ��iv���ٸ�������� ��v�������ơ�ÿ��ģ��ij�ʼ������ͬ������D��ÿ���������ʾΪ��ͼS������ÿ��ģ�⣬����ϸ������ɫ�����ڱ��Ϳռ��е�λ�����Ӧ������ˮƽ���ʾ�ǽͽ�������ˮƽ�������������Ե�������ʾ�˶�Ӧ��C2����ɫ/Ʒ��ɫ����C3����ɫ�����͵Ĺ������� E����Ӧ���������ߣ�������С����mm2Ϊ��λ�������������Ϊ��λ��ʱ�䡣ģ�ⴰ�ڣ�D���ijߴ�ԼΪ4.5��4.5 mm������IJ���ӰƬS1����
���Ǽ��������Ե������ṹ���͵ijɱ�/����ȿ����㹻�ӽ�ͳһ�ԣ������ڷ��ӻ��ĸ��С�仯�ή����Ⱥ��Ӧ�Ȳ�ѡ�����Է������Ա��͡�����ͨ����40��150��ʱͨ��ʹ��ȫ���Ի���Һʹϸ����pHe��������֮��������ڵĽ�������ѧ���Ӷ�ͨ���������������һ���衣ͼ3�Ͳ���ӰƬS1�е�ʱ��ͼ��ʾ�˴����Ͷ��յ�������̬�����վ������������Σ����ȣ�������Ⱥ�������ܵ�����Χ����ϸ��������Լ�����ڴ�Լt = 120��ʱ��C2��������С�������������Ѿ����������������������7����ͼ1��ͼ2��ʾ����t = 200��ʱ����ǰ������ԭλ������ģ������ͼ3D��ͼ2�������͵ͼ������ƾ��õ��˼�飬����������ֹС�����������͵��ݱ䣬������C3���������Ա�������Ⱥ����Ȼռ������λ����������δ��Ϊ�����Եġ���ˣ�������C2��������Ϊ�������ٽ�C3��ϸ�������ֲ�����ֹ�˽�����֢�ķ�չ����
Ȼ�����Ǽ���������е�ԭ�����еĻ����Ŷ��������C2�������Ա����Ѿ�������������������Ӧ�����ƶ���Ϊ������Ⱥ����C3����������ϸ������������Ⱥ�д��ڡ���������͵ͼ�����ȫ������Һ��������������λ������ͼ3C��ʾ������Щģ���У�δ�����Ƶ�������C2��ϸ��Ϊ�����ͼ�������Һ��ʹ�ò�δ���Ÿı���Ⱥ��̬�����ǣ���ͼ3C�Ͳ����ӰS1��ʾ���ϸ����Ļ���Һ�����Ÿı���λ���ͣ���ɫ�㣩���ر��������ƹ����У�������Ⱥ��C2��Ǩ�ƻ�C3�ࡣ��ˣ���ģ��Ԥ�⣬�ڻ�����������Խ�С���Ŷ����յ���Ⱥ��䣬���ر�ѡ������ϸ�����͡�
��TRAMP�����в���ģ��Ԥ��
����ѧģ��������������TRAMPС��������Ⱥ��̬�йص���ȷԤ�⣺��i��ԭλ����pHe��С�仯��ѡ��������Ե�C3�����ͣ��⽫��ֹ��Ϯ��֢�ķ�չ�ͣ� ii��������֢��pHe�ı�ɲ���������C3�����͵���Ⱥ��䣬�����Ž��������������ٶȡ�
����ͨ��������ˮ������200 mmol / L NaHCO3������Ԥ�⣨i�����⽫ʹǰ������pHe���ӣ�P <0.04��pHƽ��Ϊ0.2����0.04������λ��ͨ���缫�����˲�ͬŨ�ȵ�̼�����������ǰ������pHe�����ߣ�ͼ4A���������Ѫ����Ũ�ȣ�����ͼS6A����ͬ������ȫ����л�Լ��ж�����ȫ����������ǰ�о���18��21��22���й۲쵽�ģ����������ȣ��������С�����������Ų��졣��Ȼ�����Ƶ����ã�̼�����ƶ�С�����ˮ�������ˣ�����ͼS6B��S6C����
ͼ4��
��TRAMPģ���м������������� A���ڰ�����֮ǰ�������200 mmol / L̼�����δ������400 mmol / L̼�����δ����飨ÿ����n = 3��������ˮǰ���ٵ����ڲ���ֵ��ʹ�õ�ͰpH�缫MI-419��Microelectrode��Inc.������pH�����������������ˮ������ȣ���̼�����δ����Ķ����pHֵ����ͳ��ѧ�ϵ��������ӡ� *��P �� 0.015�� *��P �� 0.04����ʾ��ƽ��ֵ��SEM�� B����ͬ���Ʒ�����ǰ���������������ת����n = 5����TAP��n = 7����200 mg / L̼�����ο�ʼ���ڴ�����n = 5����200 mmol / L̼���������ڴ�����n = 5����400 mmol / L���ڴ���ͨ�����������õ�̼�����Σ�n = 7�����С�������ʾ���������о������У���4������ܸ�������400 mmol / L̼�����ƣ����Ƶ�С��ǰ�������ʼ�ձ��ּ��٣�*��P = 0.016�������������Ƶ�С��10�ܿ�ʼ�������ֳ�����24��ʱ��Ѫ������*��P = 0.03���� C��ǰ������������֯ѧ����������ʾ�ڲ�ͬ������Ⱥ��ǰ���������������ԺͶ��Ա����йص����ذٷֱȡ���Щ�����ʾ������������ȣ��ھ���4�������Ƶ�С���й۲쵽�����ԺͶ��������ٷֱ����Ų�ͬ�������ں��������ӵļ������������ơ� *��P = 0.017��*��P = 0.03��ʹ����βѧ��t����������ͳ��ѧ�����ԡ�
����ǰ�Ĺ۲�һ�£����Ƿ����ڵ�4������ȫ���Ի���Һ�ɷ�ֹ��ԭλ�����������ת�䡣 IHC�������ƺ�δ���������������������ģ�֤ʵ��C2����������δ��������Ⱥ�����Դ��ڵ����ڣ���δ������Ĥ���������ƶ����е�����ϸ�����ֳ�����������C3��أ�����ͼS7A����
��Ԥ�⣨ii�������˲��ԣ���������10����ʱ������ˮ������̼�����ƣ��Ӷ����Ѿ���C2ϸ�����ƵĽ����������н��в��ԡ�����ѧģ��Ԥ��һ�£���24�ܵ�ʱ������������ȣ���10�ܿ�ʼ��400 mmol / L̼���������Ƶ�����ʾ�����Եģ�P = 0.03������ԭ��������������ͼ4B�� ��ʬ��ʱ��IHC��ʾ�����Ƶ�������ռ������λ����Ⱥ��C3���ͣ�����ͼS2��S5������������ȣ������˿�Ǩ�Ƴ������������⣬�����ֳ�������������֯ѧ�ּ����Ž��ͣ�P = 0.03����ͼ4C����ѡ��C3���Ϳɼ���ת��
����ת����������������Ҫ��ԭ�������IJ�λ��ת�Ʋ�λ��������Ϯ��������������Ǽ���ѡ�����Ϯ��C3���ͽ����ټ̷����������γɡ�Ϊ�˶Դ˽�ģ������ͨ���ڸ������ͼ����Ͳ��������Ƶ������£������в�ͬ���͵ĵ�ϸ������������֯�����У�ģ���˻����Ʒ���һϵ��ת�����������ӵ�Ӱ�졣����ģ��ֱ��t = 120�죬��ʱ����ת�ƵĴ�С�������ͼ5A�������������ȫ���Ի���Һ������Ч����ȡ��������ʱѭ�����͵ķֲ��ʹ�С��Ȼ������ԭ��������һ������ģ��Ԥ�������ȫ���Ի���Һ����������ת����������������
ͼ5��
��TRAMPģ���м�������ת�ơ� A��δ����������ɫ���ߣ����ͼ�������ɫ����������ɫ������Һ������ת�Ƶ�ģ��������ˮƽ�������ʼת������ϸ���ı��͡���ͼ4C�ı���ͼ���ضԽǰ��ߵ�λ��ѡ�����ӣ����и�ͼ�е�0ֵ��Ӧ��λ��S���������ͣ�����ֵ1��Ӧ�������ǽͽ������ı��͡� ��ͼ4A�����Ͻǡ���Ϊ�ο�����ɫ����������ӱ��ͣ�����C3��C2ϸ�������ѱ�ǡ���ֱ����ʾת�Ƶ����մ�С����λΪmm2����ת��ϸ�����ֺ��t = 120��ʱ��������t = 0��ʼ���л����Ʒ���ֱ��ģ�������ÿ�������Ĵ����е�ƽ��ֵ��������Ʒ������������������͵�ת�ơ��ڵͼ��������£�������C2�����Ի������� B���κ�ת��ͼ�ֱ�����������ͬ�����ƶ��У��������ö����У����ǹ۲쵽��ת�ƣ�����̼���������ƵĶ����У��۲쵽����С��ת�ơ���ɫ��ͷ��������֯����ɫ��ͷ��ת�ơ� C������������ͬ���еķκ�ת�ƣ���ʾ�������ƺ�����������ķ�ת�����Ž��ͣ�**��P = 0.001���� ��*��P = 0.03�����ڸ��࣬���Ĵ���ȣ�*���������Ƶ�P = 0.01���������Ƶ�*��P = 0.02����ʾ��ƽ��ֵ��SEM��ʹ����βѧ��t����������ͳ��ѧ�����ԡ�
������Щ��ѧģ�͵Ľ��������Ȼ���о�����10��ʱ��ʼʹ�ø�������400 mmol / L����NaHCO3�Ƿ��������ת�Ƶķ�չ�����������ȣ�ת�����κε�ת�ƽ��٣��䶨����ʾ���������Լ��٣�P <0.03����ת����Ҫ�ͷŸ��ֵ���ø��������������ø��MMP���ο�����23��24����Ϊ�˼�����ڵ�MMP���ԣ�������28�ܷ���ǰ24Сʱͨ��β����ע����MMP�ɼ����ӫ��̽�루MMPSense 680����μ����Ϻͷ�����������ͼS8A�������������ȣ�ͼ��������ʾ��4�ܺ�10�ܵ�̼���������ƵĶ����У�����Խ��ͣ�P <0.05�������������ǰ�Ѿ�����������Щʵ��ķ�Χ�ڣ���Щ̽��Ļ��Բ�������pH��25����ʹ��qRT-PCR������֤����MMP-9 mRNA������C2�б����ж��������ϵ�����MMP-2��-3��-13�෴������ͼS8C����
TRAMPС��Ľ������������ʵ��ģ���и�����
Ϊ�˲������ǵĽ����TRAMPС���еĹ㷺�����ԣ����������һ��ʵ�飬��ʵ���о������ִ�л��ͬ�����ٰ�ϸ��ϵ����������MCF7�߶�������MDA-MB-231�����ھ����������⣬����֤���ˣ�����ͼS9A�CS9C����MDA-MB-231ϸ�����кܸߵ��ǽͽ��ԣ�P <0.0001�������ᣬ�ܶ��Ժ���C2ϸ�����Ƶ���Ϯ�ԣ���MCF7ϸ�������ֺ��ԣ����ܶ��ԣ������ֳ���C3ϸ�����ƵĽ��������������Ǵ�л�� IHC�����ʾ����MCF7ϸ����ȣ����Գ̶ȸ��ߵ�MDA-MB-231������֯��GLUT-1�������ߣ�P = 0.0013��������ͼS9D�������Ǹ�����MCF7��MDA-MB-231ϸ�����ֱ����eGFP�ͺ�ɫӫ�⵰�ף�RFP���������⣬������������Ⱥ�γ������壬������л�û��Matrigel������¾���Ͼ��ȣ�ÿ��������n = 8��������Сʱ�ڣ�ϸ��Ѹ���ƶ��������˶��ض�һ�µĿռ���״̬��MDA-MB-231ϸ���γ�������ı��棬MCF7��MCF7ϸ��������������������ڣ�����ͼS10��������������ϸ��ϵ�ij�ֻ�ϵ�ϸ������ͬ������ע�䵽����SCIDС�������֬�����С�������ע��֮ǰ���Ƽ��س�����Ƥ�·���������ER + MCF7ϸ����������Ե�GFP��RFPӫ�����ڶ��Լ����Щ�����������������ȷ���˽����յ��������ʵ�ʱ�䡣ֲ��21����������ͨ��IHC����Ƭ��ER�������֣��Լ���Ⱥ���е�MCF7ϸ��������Щ�о��У���ER�����IHC��������ѡ���յ㣬��Ϊ����CLIA�����о��кܸߵ������ԣ����ҿ����������صķ�ʽ�Զ����Ʒ�ʽ���ж������෴�����ڹ�Ĵ���ɢ���Լ�������pH����������ӫ�⵰�׳������֪Ӱ�죬GFP��RFPӫ�������������ڶ��ն����У�ER- MDA-MB-231ϸ�����յ����Ҫ��Ⱥ�����ǣ�����400 mmol / L NaHCO3������С���У��������ER + MCF7ϸ�������������ӣ�P <0.0001����ͼ6A��B������ͼS11�������⣬��Ⱥ������������������ʽ���ͬʱ������ͼ6C����
ͼ6��
A������ͼ�����ڲ�ͬ������ÿ��ϸ��ϵ�ͻ���MDA-MB-231��MCF7��1��1���Ĵ�����������H��Eͼ����ͼ����H��E����ͬ������������Ƭ��ERȾɫ�� B���ڸ�ʵ����ʹ�õ�����������ER����ķ�������ע�⣬��̼������400 mmol / L��������Щ��������MDA-MB-231��MCF7�Ļ���1��1��ɣ����е�ER����Ҫ������ˮ�еĸ���P = 0.0001���� C����ʵ����ʹ�õ�����������MRI������ݡ����ݱ�ʾΪ����������������ע��������ı仯��������ʾ��ƽ��ֵ��SEM��ʹ����βѧ��t����������ͳ��ѧ�����ԡ�
ͼ7��
��̬λ����������Բ���ģ�͡����ǵļ����ǣ�������������ͬ��ϸ����Ⱥ��ɣ��߶��ǽͽ�IJ���ϸ������ϸ�����ͷ��ǽͽ�ķDz���ϸ������ϸ���������ǵ�ģ��Ԥ�⣬pHe��С�Ŷ����ܻ��յ���Ⱥ��䣬�Ӷ������ڷDz��ᣬ����Ϯ��֢��Ⱥ�� PIN��ǰ������Ƥ�����䡣
��ˣ����ǵ�ģ�ͱ������������е�������Ⱥ��ʾ��C2���͵Ĵ�л����Ϯ���ԣ������ƶ����е���������Ⱥ������ֳ�C3���ͣ������������С����֯ѧ�ּ���ת�Ƶ�Ӱ��һ�£�ͼ7������
��Ȼ�������ڽ��������˶���Ŵ�����ľ�����Ⱥ������������о�����Щ��Ⱥ����Ӧ���ԣ����ܿ����кܶ࣬�����Dz����ڴ����ֲ�ͬ���Է�����ģ����ȡ�������������ȶ�ά�ֵ����ֱ��͡�
ÿ���˶�����Ƶ��ص���̬ϵͳ���Դٽ���������ɢ���ƻ��������֡�Ѫ�����ɱ��ʹٽ�Ѫ���������������ӳ���������������ֳ�����ǣ��ñ��ʹٽ���Խ��պͻ���������������ģ��Ԥ���롰�ƶ���������Ե����֯ѧ�۲���һ�£�ͨ�����Դ������õ�Ԥ��26�����෴��ͨ���ữ�����������Ա�����������鵼�ľ�����ϸ����Ӧ���Ե����ƣ����ƶ�������ԭ������Ӧ���Լ�ϸ������ʵĽ��⣬�Ӷ��ٽ������֡���ǰ���о����������ӵIJ���������������أ�27���������ȫ�����������������������ǽͽ���ϸ���˶�֮����ڸ߶�����ԣ�28��������֯ѧ�Ͻ����ñ��ͱ���Ϊ�����߽磬Ԥ������26����
�����ڽ��е������ڽ����У�ÿ����Ӧ���Ե��洦����ɱ�����Ȩ�⡣���������Բ��ԣ��ɱ��������������ǽͽ����Ӧ���Ի����Ĵ�л�������磬����Ĥ���ӱã������µ���������Ч�ʽ��͡����ھ������ԭ���Ժ�ת����֢��FdG PET��������ʾ��Խ��Խ��������������������������ĺô��ƺ�ͨ���ᳬ���ɱ���
����������ʣ��������Ե����ƶ��ⲿ�����ж�ǿ�����ӵĶ���ѧϵͳ�����簩֢��ͨ���ɷ����Խ���������������Щ����ѧ����ֱ�۵�Ԥ�⡣��ˣ�ʵ�鹤��������ѧģ�͵�ָ���½��еģ��������ʹpHe��С�仯Ҳ���ܽ����������ǽͽ���͵���Ӧ�����ƣ�������Ⱥ��䣨ͼ3���������ڷDz���������Ա��͡���
��TRAMPС����֤ʵ����һԤ�⣬��Ϊǰ�����ڻ�������pHe��С�仯�ٽ��˷������Ա��Ͳ����Ÿı���������������ʽ��Ϊ����ȷ�о���������Ӧ�Բ���֮��ľ���������ʹ���������ٰ�ϸ��ϵ������һ��ʵ��������������Ϯ�ԣ���л�ӽ�������Ѫ�����ɵ�MCF7ϸ������Ϯ�ԣ��߶��ǽͽ⣬�������MDA-MB-231ϸ������TRAMPС���е�ģ��Ԥ��۲���һ�£����Ƿ���MDA-MB-231ϸ����Ϊ���ڵ�������Ⱥ�����ǣ���������ˮ������400 mmol / L NaHCO3�ظ�����ʵ��ʱ��MCF7ϸ������ܳ裬�������������Լ�����ͼ6������ͼS11����
�ܶ���֮������֤�������������ӵĶ���ϵͳһ����ͨ��Ӧ����Խ�С���߶�ѡ���Ե�����ѧ�����������Խ���֢�����������Խϵ͵Ĺ����С���ʹû�ж�ÿ����ɲ��ֵ�ȫ���˽⣬Ҳ����ʵ����һĿ�ꡣͨ��Ӧ����ѧģ�Ͳ���ϵͳ�еĹؼ������Է����Դ���Ķ���ѧ��Defining Cancer Subpopulations by Adaptive Strategies Rather Than Molecular Properties Provides Novel Insights into Intratumoral Evolution
Arig Ibrahim-Hashim, Mark Robertson-Tessi, Pedro M. Enriquez-Navas, Mehdi Damaghi, Yoganand Balagurunathan, Jonathan W. Wojtkowiak, Shonagh Russell, Kam Yoonseok, Mark C. Lloyd, Marilyn M. Bui, Joel S. Brown, Alexander R.A. Anderson, Robert J. Gillies and Robert A. Gatenby
DOI: 10.1158/0008-5472.CAN-16-2844 Published May 2017
Abstract
Ongoing intratumoral evolution is apparent in molecular variations among cancer cells from different regions of the same tumor, but genetic data alone provide little insight into environmental selection forces and cellular phenotypic adaptations that govern the underlying Darwinian dynamics. In three spontaneous murine cancers (prostate cancers in TRAMP and PTEN mice, pancreatic cancer in KPC mice), we identified two subpopulations with distinct niche construction adaptive strategies that remained stable in culture: (i) invasive cells that produce an acidic environment via upregulated aerobic glycolysis; and (ii) noninvasive cells that were angiogenic and metabolically near-normal. Darwinian interactions of these subpopulations were investigated in TRAMP prostate cancers. Computer simulations demonstrated invasive, acid-producing (C2) cells maintain a fitness advantage over noninvasive, angiogenic (C3) cells by promoting invasion and reducing efficacy of immune response. Immunohistochemical analysis of untreated tumors confirmed that C2 cells were invariably more abundant than C3 cells. However, the C2 adaptive strategy phenotype incurred a significant cost due to inefficient energy production (i.e., aerobic glycolysis) and depletion of resources for adaptations to an acidic environment. Mathematical model simulations predicted that small perturbations of the microenvironmental extracellular pH (pHe) could invert the cost/benefit ratio of the C2 strategy and select for C3 cells. In vivo, 200 mmol/L NaHCO3 added to the drinking water of 4-week-old TRAMP mice increased the intraprostatic pHe by 0.2 units and promoted proliferation of noninvasive C3 cells, which remained confined within the ducts so that primary cancer did not develop. A 0.2 pHe increase in established tumors increased the fraction of C3 cells and signficantly diminished growth of primary and metastatic tumors. In an experimental tumor construct, MCF7 and MDA-MB-231 breast cancer cells were coinjected into the mammary fat pad of SCID mice. C2-like MDA-MB-231 cells dominated in untreated animals, but C3-like MCF7 cells were selected and tumor growth slowed when intratumoral pHe was increased. Overall, our data support the use of mathematical modeling of intratumoral Darwinian interactions of environmental selection forces and cancer cell adaptive strategies. These models allow the tumor to be steered into a less invasive pathway through the application of small but selective biological force. Cancer Res; 77(9); 2242�C54. ©2017 AACR.
Major Findings
Defining intratumoral subpopulations by their adaptive strategies rather than the molecular properties used in branching clonal evolution models allows the cellular and environmental interactions to be identified and framed mathematically. With sufficient understanding of the underlying eco-evolutionary forces, the tendency of complex dynamic systems to magnify small perturbations can be exploited to steer a tumor into a noninvasive growth regime by applying relatively small biological perturbations.Defining Cancer Subpopulations by Adaptive Strategies Rather Than Molecular Properties Provides Novel Insights into Intratumoral Evolution | Cancer Research
https://cancerres.aacrjournals.org/content/77/9/2242��
Published: 01 November 2004
Why do cancers have high aerobic glycolysis?
Robert A. Gatenby & Robert J. Gillies
Abstract
If carcinogenesis occurs by somatic evolution, then common components of the cancer phenotype result from active selection and must, therefore, confer a significant growth advantage. A near-universal property of primary and metastatic cancers is upregulation of glycolysis, resulting in increased glucose consumption, which can be observed with clinical tumour imaging. We propose that persistent metabolism of glucose to lactate even in aerobic conditions is an adaptation to intermittent hypoxia in pre-malignant lesions. However, upregulation of glycolysis leads to microenvironmental acidosis requiring evolution to phenotypes resistant to acid-induced cell toxicity. Subsequent cell populations with upregulated glycolysis and acid resistance have a powerful growth advantage, which promotes unconstrained proliferation and invasion.
Key Points
Widespread clinical use of 18fluorodeoxyglucose positron-emission tomography has demonstrated that the glycolytic phenotype is observed in most human cancers.
The concept of carcinogenesis as a process that occurs by somatic evolution clearly implies that common traits of the malignant phenotype, such as upregulation of glycolysis, are the result of active selection processes and must confer a significant, identifiable growth advantage.
Constitutive upregulation of glycolysis is likely to be an adaptation to hypoxia that develops as pre-malignant lesions grow progressively further from their blood supply. At this stage, the blood supply remains physically separated from the growing cells by an intact basement membrane.
Increased acid production from upregulation of glycolysis results in microenvironmental acidosis and requires further adaptation through somatic evolution to phenotypes resistant to acid-induced toxicity.
Cell populations that emerge from this evolutionary sequence have a powerful growth advantage, as they alter their environment through increased glycolysis in a way that is toxic to other phenotypes, but harmless to themselves. The environmental acidosis also facilitates invasion through destruction of adjacent normal populations, degradation of the extracellular matrix and promotion of angiogenesis.
We propose that the glycolytic phenotype, by conferring a powerful growth advantage, is necessary for evolution of invasive human cancers.
Why do cancers have high aerobic glycolysis? | Nature Reviews Cancer
https://www.nature.com/articles/nrc1478��
Cell Cycle. 2019 Jun;18
Proliferating tumor cells mimick glucose metabolism of mature human erythrocytes
Mehrdad Ghashghaeinia 1, Martin Köberle 2, Ulrich Mrowietz 1, Ingolf Bernhardt 3
1a Department of Dermatology , University Medical Center Schleswig-Holstein, Campus Kiel , Kiel , Germany.
2b Klinik und Poliklinik f��r Dermatologie und Allergologie, Fakultät f��r Medizin , Technische Universität M��nchen , Munich , Germany.
3c Laboratory of Biophysics, Faculty of Natural and Technical Sciences III , Saarland University , Saarbruecken , Germany.
Abstract
Mature human erythrocytes are dependent on anerobic glycolysis, i.e. catabolism (oxidation) of one glucose molecule to produce two ATP and two lactate molecules. Proliferating tumor cells mimick mature human erythrocytes to glycolytically generate two ATP molecules. They deliberately avoid or switch off their respiration, i.e. tricarboxylic acid (TCA) cycle and oxidative phosphorylation (OXPHOS) machinery and consequently dispense with the production of additional 36 ATP molecules from one glucose molecule. This phenomenon is named aerobic glycolysis or Warburg effect. The present review deals with the fate of a glucose molecule after entering a mature human erythrocyte or a proliferating tumor cell and describes why it is useful for a proliferating tumor cell to imitate a mature erythrocyte. Blood consisting of plasma and cellular components (99% of the cells are erythrocytes) may be regarded as a mobile organ, constantly exercising a direct interaction with other organs. Therefore, the use of drugs, which influences the biological activity of erythrocytes, has an immediate effect on the entire organism.ϸ������Cell Cycl.2019��6��18��
����������ϸ��ģ�³��������ϸ���������Ǵ�л
Mehrdad Ghashghaeinia 1, Martin Koberle 2, Ulrich Mrowietz 1, Ingolf Bernhardt 3
ʯ�������-�ɶ�˹̩���ѧҽѧ����Ƥ����1a��������У�����������¹���
�¹�Ľ��ڹ�ҵ��ѧ��Klinik��Poliklinik fur Dermatologie��Allergologie, Fakultat fur Medizin
�¹�������ѧ��Ȼ�뼼����ѧϵ��������3cʵ���ң�������³�ϡ�
ժҪ
����������ϸ�������������ǽͽ⣬��һ�������Ƿ��ӵķֽ�(����)��������ATP������������ӡ���ֳ������ϸ��ģ�³���������ϸ�������ǽͽ�����в�������ATP���ӡ����ǹ�������ر����ǵĺ������ã���������(TCA)ѭ�����������ữ(OXPHOS)���ƣ��Ӷ������һ�������Ƿ��Ӳ��������36��ATP���ӡ���������Ϊ�����ǽͽ���߲���ЧӦ��Ŀǰ���������������Ƿ��ӽ��������˺�ϸ������ֳ������ϸ��������ˣ�������Ϊʲô�������õ���ֳ������ϸ��ģ�³���ĺ�ϸ������Ѫ����ϸ����ɵ�ѪҺ(99%��ϸ���Ǻ�ϸ��)���Կ�����һ���ƶ������٣����ϵ����������ٷ���ֱ�ӵ�����á���ˣ�Ӱ���ϸ��������Ե�ҩ���ʹ�ã����������������ͼ�Ӱ��Ӱ�졣https://pubmed.ncbi.nlm.nih.gov/31154896/
��


%20v.jpg)

.jpg)